こんにちは。谷川(脳神経内科専門医)です。
『iPS細胞研究の軌跡と実用化への道筋(医学界新聞プラス2025年)』
この記事は、京都大学iPS細胞研究所(CiRA)で行われたパーキンソン病に対するiPS細胞を用いた再生治療(治験)結果および治験に至るまでの経緯などを含み、興味深い内容であったのでした。
この記事をきっかけにいろいろと自分なりに調べて理解したことをお話しします。
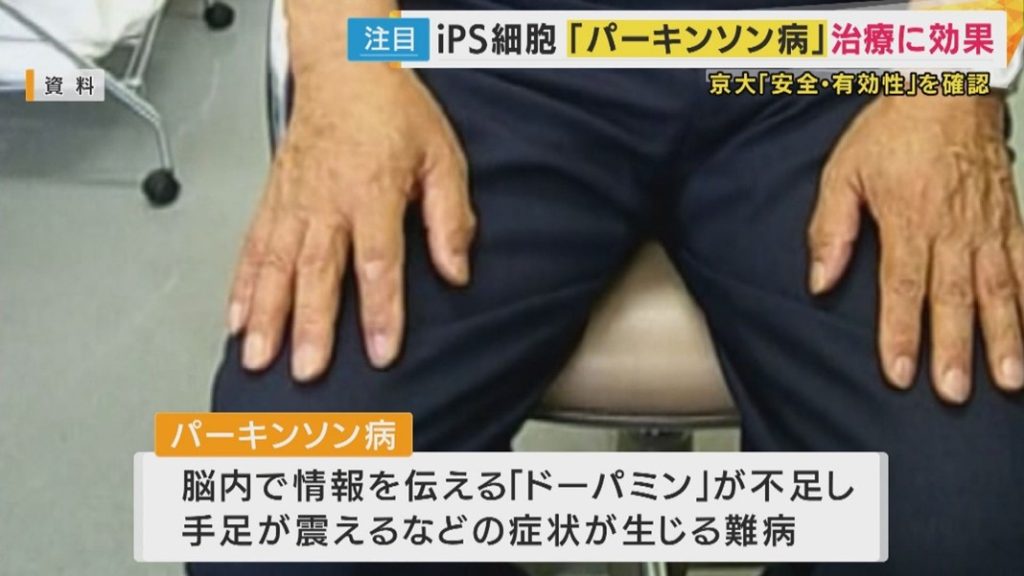
まず、パーキンソン病がなぜ発症するのかについて。
脳の中の中脳黒質(ちゅうのうこくしつ)にあるドパミン神経細胞でドパミンがつくられ、これが次の神経へと伝えられることによって人間の動きを調整しています。
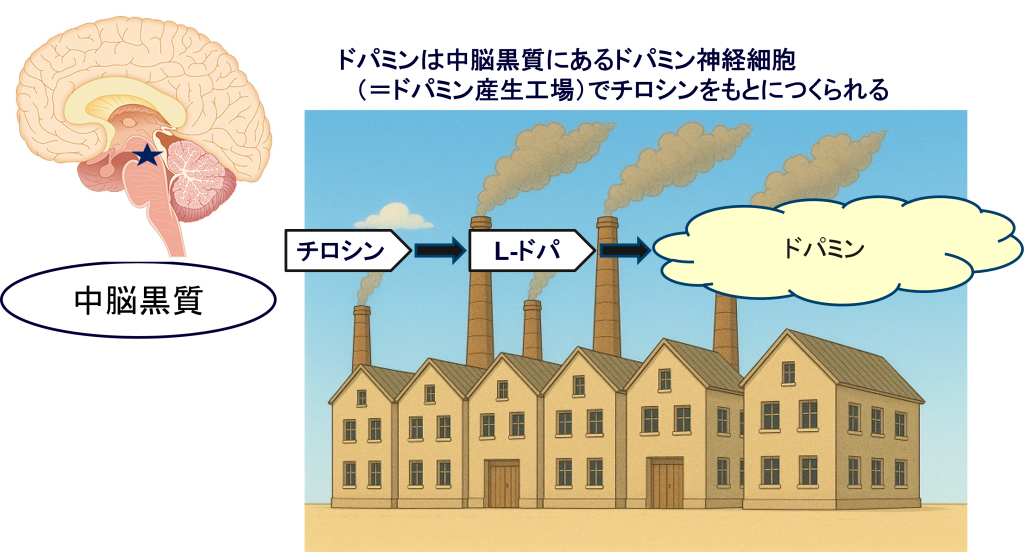
ところがパーキンソン病の患者さんの脳ではドパミン神経細胞に
『レビー小体』が発現し細胞障害→ドパミン神経細胞減少→ドパミン低下をきたし、動きの障害が起きます。

現在の治療法としては、ドパミンの材料となるL-ドパを飲み、細胞障害を受けていない残ったドパミン神経細胞でドパミンを作らせる治療です。
ドパミン神経細胞を工場に例えると、一部壊れている工場に材料(L-ドパ)を多めに送り込み、なんとかドパミン産生量を上げようという治療です。

しかし、病気の進行とともにドパミン神経細胞はさらに壊れていき、L-ドパを多く内服しても、ドパミンがほとんど作られなくなってしまいます。
そこで、ドパミン神経細胞そのものを再生する治療が考えられました。
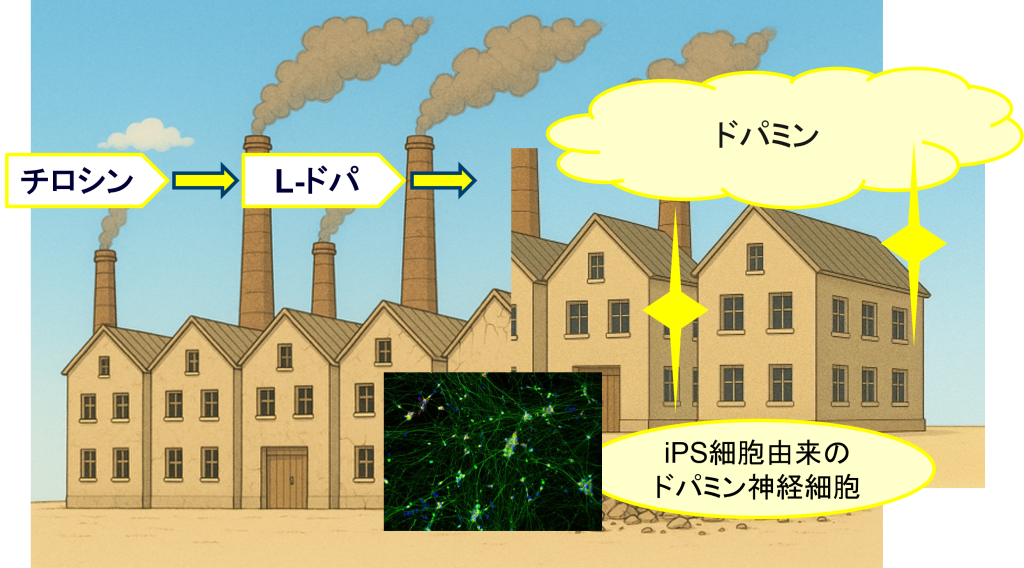
もともと海外で1980年代末から胎児の中脳からドパミン神経細胞を取り出し、患者さんの脳に移植するという治療が行われ、約400例についてある程度効果が認められた例がありました。しかし、倫理的な問題や必要な多くの細胞を集めるが難しい、などの側面がありました。
そこで細胞を大量に集められるものとしてES細胞やiPS細胞といった多能性幹細胞が注目されました。
ES細胞(胚性幹細胞)は、受精卵から作られる多能性幹細胞で受精卵と同じように体を構成するあらゆる細胞へと変わる能力(多分化能)を持ち、再生医療に対する応用がされています。
日本では、2019年に国立成育医療研究センターにおいて、肝疾患(先天性尿素サイクル異常症)新生児に対し、ES細胞由来の肝細胞移植が行われ成功しています。
しかし、ES細胞は、他者のHLA(ヒト白血球抗原)が入るため拒絶反応のリスクがあり、受精卵を壊して細胞を採取するため倫理的な問題も包含しています。
一方、iPS細胞は、患者さん自身の細胞(皮膚など)をもとに作れるので拒絶反応や倫理的問題は少ないとされます。
iPS細胞の作製についてですが、患者さん自身の体細胞に多能性誘導因子(遺伝子(Oct3/4, Sox2, Klf4, c-Myc)など(作成者により異なる))を導入・培養することによって細胞のリプログラミングを起こしてできます。(山中伸弥ら. Cell,2007)
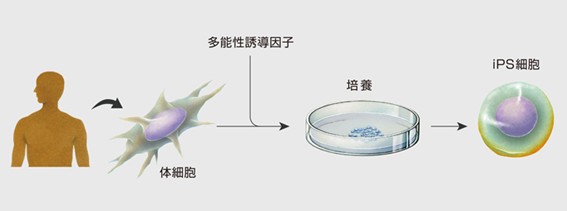
近年、iPS細胞による再生医療は、パーキンソン病のような神経難病にも向けられています。しかし、『細胞の選別』や『移植細胞の生着性』などいくつかの問題点がありました。

まずiPS細胞を分化誘導してできた神経幹細胞の中からドパミン神経細胞だけを選別する技術の改良(土井大輔ら.Stem Cell Reports,2014)が行われ、
過剰な増殖が抑えられました。
また移植先の脳の環境についてもiPS由来ドパミン神経細胞が生着しやすくし、移植効果を高める研究も進みました。
こうした段階を経て、2018~23年にかけて7人のパーキンソン病患者を対象とした、iPS細胞由来のドパミン神経細胞移植の治験が行われました。
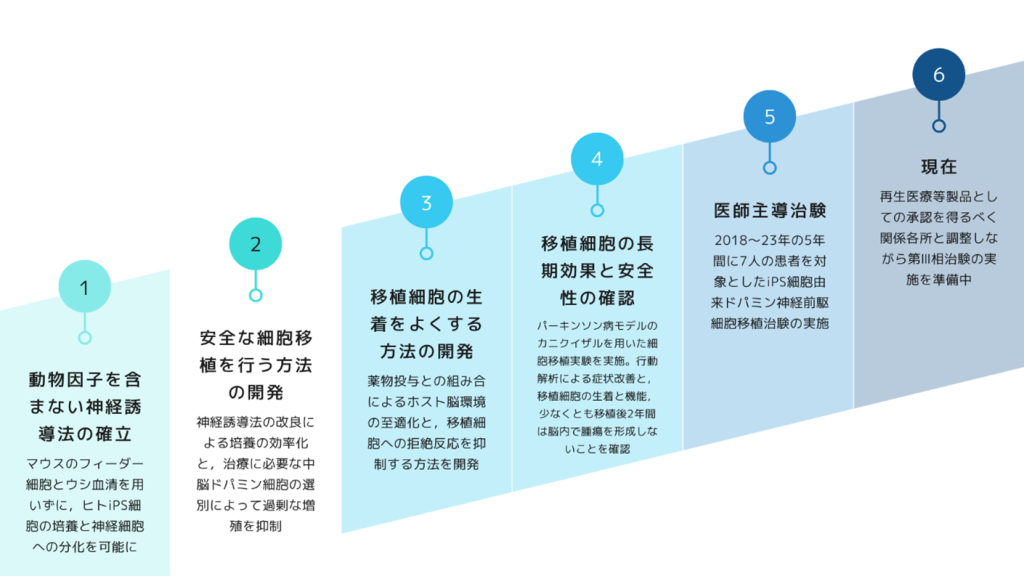
その結果、参加した7人全員において移植した細胞に癌化は認めず安全性が確認されました。
またそのうち6人で有効性の評価も行われ、いずれも移植したドパミン神経細胞からドパミンがでていることが確認され、このうち4人では、運動機能の改善が認められました。
この明るい結果から、治験で神経細胞の製造を担った製薬会社は、実用化を目指して厚生労働省に承認申請を行う方針、と報じられています。
いままで、ドパミン内服治療を長年行っても、徐々に薬の効果がなくなり、寝たきりになっていく患者さんたちを多くみてきましたが、
iPS細胞を用いた再生治療により、一度は失われた機能を回復し、時間を巻き戻すかのように治っていく、そんな神経難病治療の未来が近づいているのではと感じました。






